2022年11月21日,国际知名期刊《自然-通讯》在线发表了我校陈忠教授/汪仪研究员团队题为“激活的星形胶质细胞通过驱动Na+-K+-ATPase减轻啮齿动物模型中的新皮质癫痫发作”的研究成果(Nat Commun, 2022b)。该团队长期从事癫痫的发病机制解析与治疗药物靶点的发现研究,前期重点关注癫痫发病中以海马下托为核心的神经环路“兴奋-抑制”平衡机制与调控治疗新策略(Neuron, 2017; Ann Neurol, 2019, 2021; Biol Psychiat, 2020; Nat Nanotech, 2020; Nat Commun 2020, 2022a; iScience 2022; Sci Adv, 2022)。本研究在前期研究的基础上,进一步揭示星形胶质细胞参与癫痫发作的机制,研究发现通过光遗传学手段特异性激活皮层星形胶质细胞的Na+-K+-ATPase功能,从而达到治疗新皮层癫痫的效果,为癫痫治疗提供了新的思路和潜在靶点。

癫痫是神经系统最常见的疾病之一,困扰了全球近1%的人口,并有近三分之一的患者症状难以被抗发作药物控制而成为耐药性癫痫。皮层癫痫是其中常见的耐药性癫痫类型,针对其发作机制及治疗新策略的研究尤为迫切。
目前人们对于癫痫发作机制的研究主要集中在神经元的“兴奋-抑制”失衡上,现有的抗癫痫药物研发也几乎全是以神经元为作用靶点。近年来,越来越多的观点认为“星形胶质细胞-神经元”的相互作用在癫痫中扮演了重要角色。然而研究人员因一直无法明确星形胶质细胞在癫痫发生和发展过程中的角色而难以有效地针对这一相互作用而开发药物,主要归因于目前缺少特异性的手段调控星形胶质细胞,精准区分开星形胶质细胞对周围神经元的影响。
本研究中,研究人员将光敏感通道蛋白 ChR2特异性地表达在小鼠/大鼠运动皮层的星形胶质细胞中,首次发现用光选择性激活星形胶质细胞,可以有效抑制皮层癫痫的发生和发展。重要的是,与传统的直接抑制神经元相比,光遗传学激活星形胶质细胞所展现的抗癫痫作用具有以下几个优势:(1)抗癫痫作用的治疗窗宽,在癫痫发病的早期或是晚期进行光遗传学激活星形胶质细胞均可以产生治疗作用;(2)抗癫痫作用空间范围广泛,在癫痫灶点的远侧激活星形胶质细胞仍可以有效降低癫痫发作;(3)抗癫痫作用的同时对正常生理功能无明显影响。
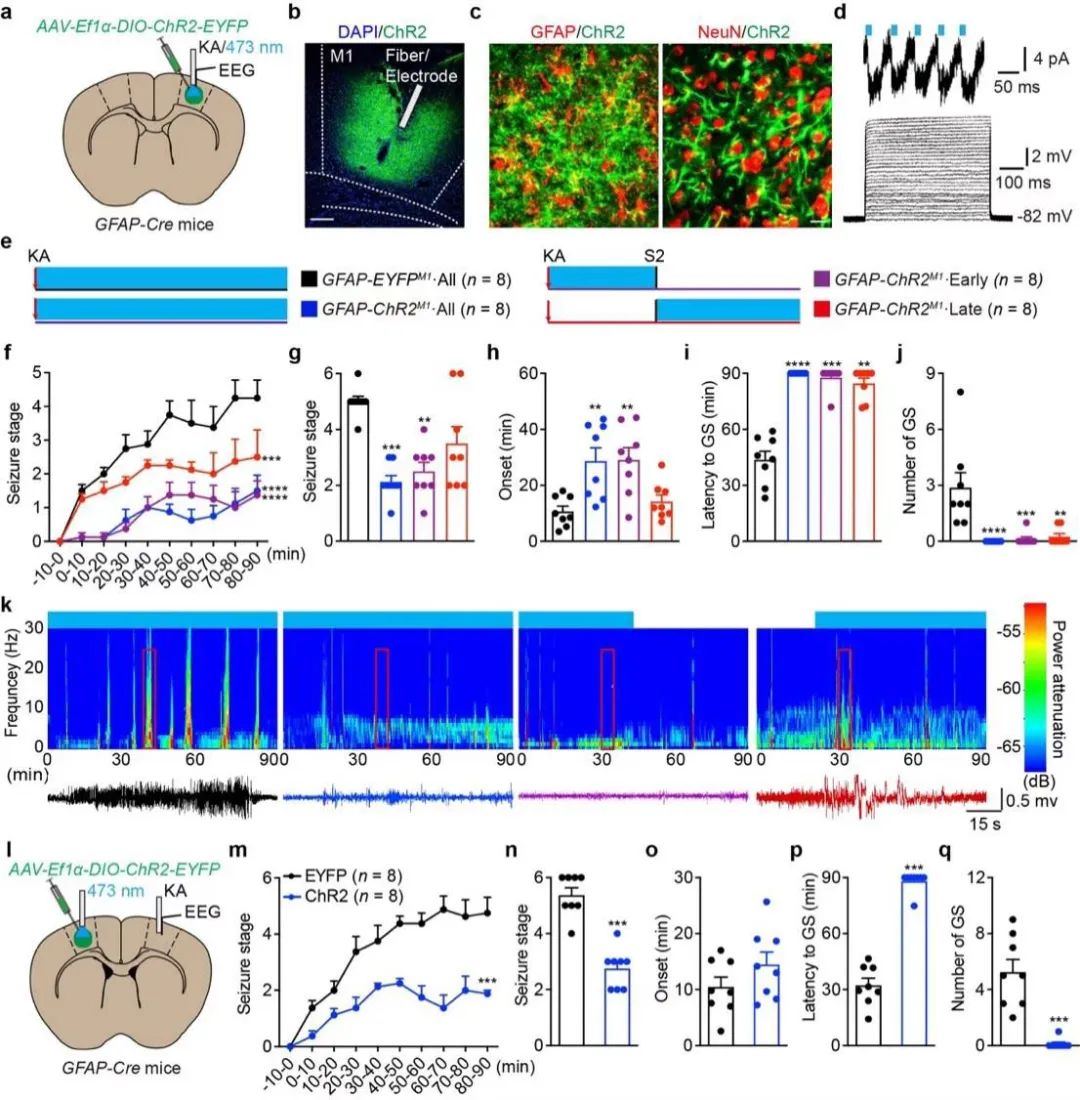
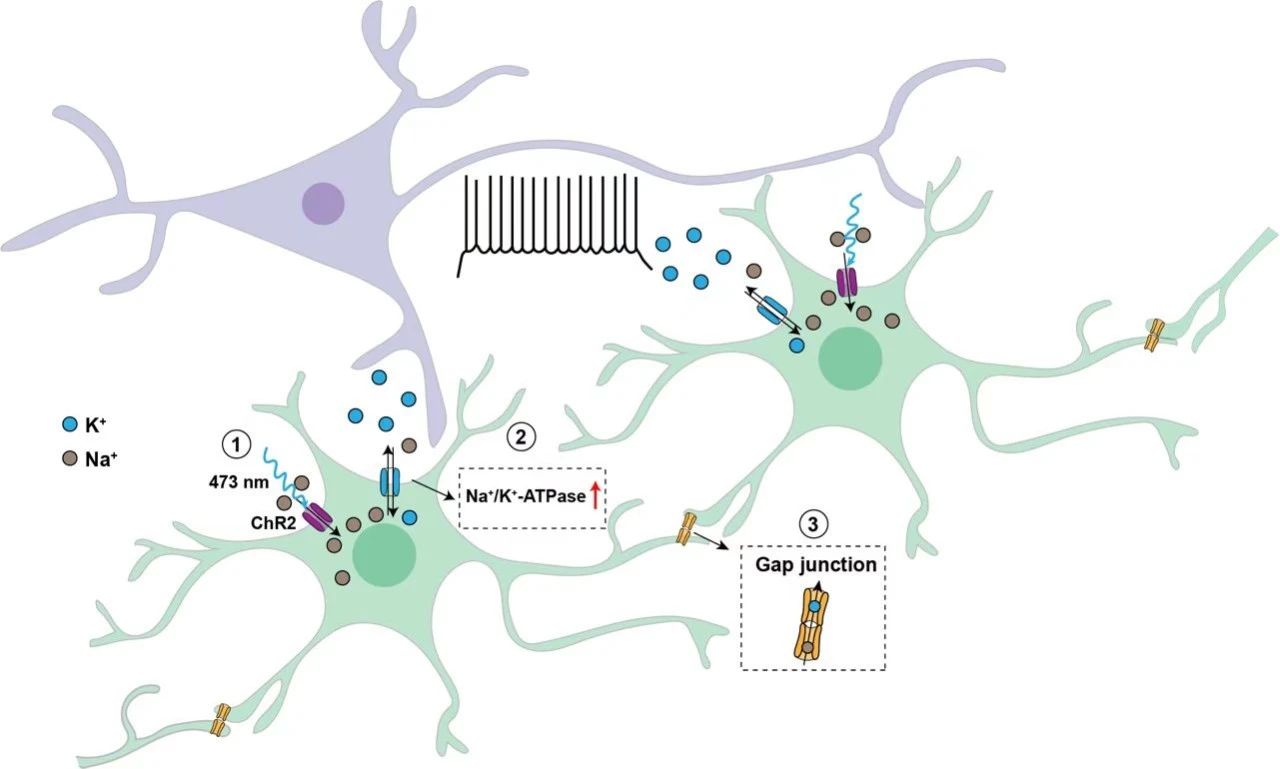
机制上,本研究进一步发现光遗传学激活星形胶质细胞可以活动依赖性地抑制癫痫发作中的高频放电的锥体神经元。这一作用与经典的星形胶质细胞Ca2+介导的胶质递质无关,而是与星形胶质细胞上Na+-K+- ATPase功能增强。Na+-K+- ATPase功能增强可以介导的癫痫发作时细胞外高浓度钾离子缓冲,从而降低神经兴奋性密切相关。这种效应可以进一步通过星形胶质细胞之间的缝隙连接所形成的广泛网络发挥抗持久和广泛的抗癫痫作用。
本研究第一作者为赵俊利博士和硕士生孙进一,陈忠教授和汪仪研究员为共同通讯作者。研究受到了国家科技部重点研发计划课题、国家自然科学基金优青项目、浙江省自然科学基金重大项目等项目资助。




